Η φαρμακευτική εταιρεία Moderna ανακοίνωσε σήμερα ότι υπέβαλε στον FDA ένα αίτημα για πλήρη έγκριση του εμβολίου
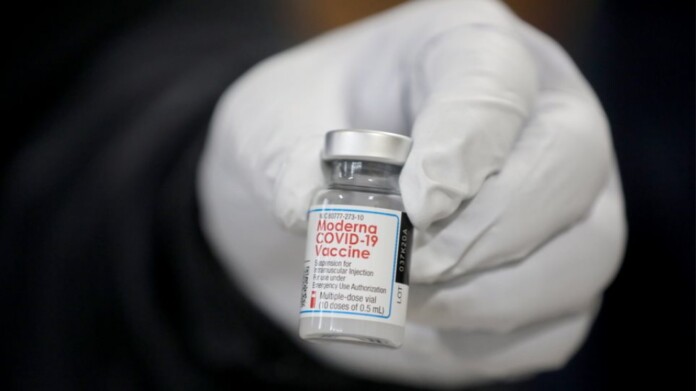
Η φαρμακευτική εταιρεία Moderna ανακοίνωσε σήμερα ότι υπέβαλε στον Αμερικανικό Οργανισμό Φαρμάκων και Τροφίμων (FDA) ένα αίτημα για πλήρη έγκριση του εμβολίου της για την Covid-19 για άτομα ηλικίας 18 ετών και άνω.
Το εμβόλιο έλαβε στις 18 Δεκεμβρίου άδεια κατεπείγουσας χρήσης από τον FDA, διαδικασία που κατέστησε δυνατή την ταχεία αντίδραση απέναντι στην υγειονομική κρίση.
Από τότε έχουν χορηγηθεί περισσότερες από 124 εκατομμύρια δόσεις του εμβολίου της Moderna σε ολόκληρη τη χώρα, σύμφωνα με τα στοιχεία των Κέντρων Ελέγχου και Πρόληψης Νοσημάτων (CDC), την κύρια ομοσπονδιακή υπηρεσία δημόσιας υγείας των ΗΠΑ.
Μια άδεια κατεπείγουσας χρήσης βασίζεται «στα βέλτιστα διαθέσιμα στοιχεία» χωρίς την αναμονή για μακροπρόθεσμα δεδομένα παρακολούθησης, απαραίτητα για πλήρη έγκριση, εξηγεί ο FDA στον ιστότοπό του.
Αυτού του τύπου η άδεια έκτακτης ανάγκης, που χορηγείται υπό όρους, μπορεί να ανακληθεί ή να τροποποιηθεί ανά πάσα στιγμή, ανάλογα με τα νέα δεδομένα που συλλέγονται.
«Είμαστε στην ευχάριστη θέση να ανακοινώσουμε αυτό το σημαντικό βήμα», ανέφερε σε ανακοίνωσή του ο διευθύνων σύμβουλος της Moderna, Στεφάν Μπανσέλ.
Η αμερικανική εταιρεία βιοτεχνολογίας «θα συνεχίσει να παρέχει δεδομένα (…) συνεχώς μέσα στις επόμενες εβδομάδες» στις υγειονομικές αρχές, προκειμένου να στηρίξει το αίτημά της, συμπλήρωσε.
Η συμμαχία Pfizer/BioNTech υπέβαλε επίσης στις αρχές Μαΐου στον FDA αίτημα για πλήρη έγκριση για το δικό της εμβόλιο για την Covid-19, για άτομα ηλικίας 16 ετών και άνω.